Saizen 12 mg/1,5 mL (somatropina) con lote AU029639 y fecha de caducidad 08/2024 no fue fabricado por Merck Biopharma
Por Félix Muñiz
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) ha lanzado una alarmante advertencia sobre la presencia en el mercado mexicano de productos falsificados de Saizen, una somatropina utilizada para el tratamiento de déficits hormonales y trastornos del crecimiento.
Según la investigación realizada por Merck Biopharma Distribution, se han identificado varios lotes de Saizen 12 mg/1,5 mL (somatropina) que no fueron fabricados ni distribuidos por la empresa. En particular, el lote AU029639 con fecha de caducidad 08/2024 presenta etiquetas con textos en idioma diferente al español y carece del registro sanitario requerido, lo que pone en duda su autenticidad y seguridad para los pacientes.
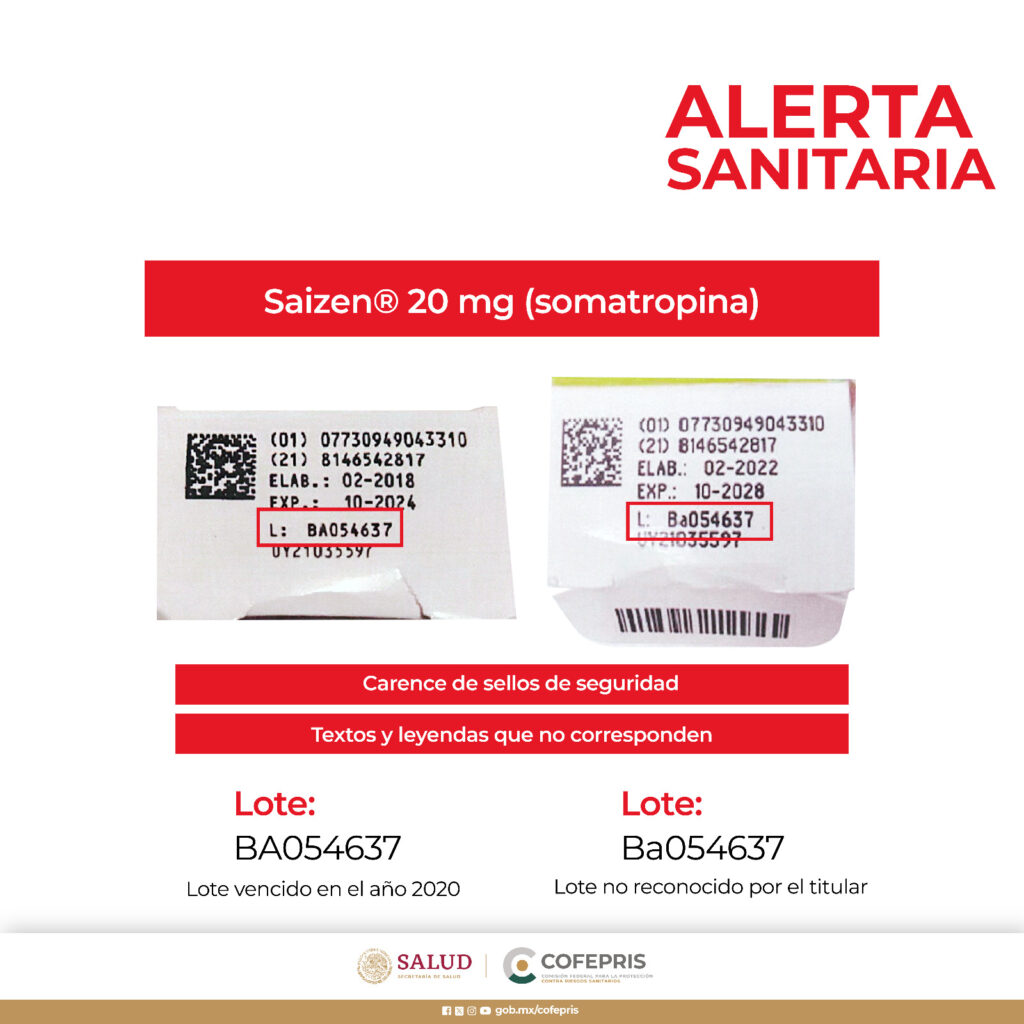
Además, los lotes BA054637 y Ba054637 de Saizen 20 mg (somatropina) han mostrado irregularidades significativas en su etiquetado, incluyendo la ausencia de sellos de seguridad y textos también en idioma diferente al español, lo cual dificulta la trazabilidad y garantía de su origen y calidad.
El uso de estos productos falsificados representa un grave riesgo para la salud pública debido a la incertidumbre respecto a sus ingredientes, condiciones de fabricación, almacenamiento y transporte. Cofepris enfatiza que no puede garantizar la eficacia, calidad ni seguridad de estos medicamentos, por lo que insta a la población a evitar su adquisición y uso.
Las entidades identificadas como distribuidoras de estos productos irregulares incluyen a Efarma Centro Médico, Educación Especial y Comercializadora de Fármacos Especializados, así como a Capital Nutrition. Estas empresas están listadas como distribuidores que han incumplido con la regulación sanitaria vigente, según la Plataforma de distribuidores irregulares de medicamentos de Cofepris.
Ante esta situación, Cofepris recomienda a los consumidores verificar la autenticidad de cualquier medicamento Saizen contactando directamente al titular del registro sanitario correspondiente. Esta información está disponible en la página oficial de Consulta de registros sanitarios de Cofepris.
En caso de haber utilizado alguno de los medicamentos con los lotes y fechas de vencimiento mencionados y experimentar cualquier síntoma adverso, reacción o malestar, se insta a los usuarios a reportarlo a través del enlace proporcionado en línea. Para mantenerse informado sobre otras alertas sanitarias y productos riesgosos, se recomienda visitar regularmente la página del Sistema de Alertamiento Sanitario.
Finalmente, Cofepris hace un llamado a los distribuidores y puntos de venta para que retiren del mercado cualquier medicamento con fecha de caducidad vencida o próxima a vencer, y adquieran productos únicamente de proveedores autorizados y validados por las autoridades competentes. Es esencial que estos proveedores cuenten con licencia sanitaria vigente, aviso de funcionamiento y la documentación que asegure la legalidad en la adquisición y distribución de productos farmacéuticos.
La Comisión Federal reitera su compromiso con la vigilancia sanitaria y se compromete a mantener informada a la población sobre nuevas evidencias o riesgos relacionados con la salud pública, con el objetivo de evitar que productos fraudulentos o empresas irresponsables pongan en peligro la salud de los mexicanos.
Esta alerta se emite con fines informativos y de protección a la salud pública, sin implicar una resolución administrativa definitiva.

